Бронхиальная астма
ОПРЕДЕЛЕНИЕ И КЛАССИФИКАЦИЯ
Бронхиальная астма - это хроническое воспалительное заболевание дыхательных путей, в котором принимают участие многие клетки и клеточные элементы. Хроническое воспаление обусловливает развитие бронхиальной гиперреактивности, которая приводит к повторяющимся эпизодам свистящих хрипов, одышки, чувства заложенности в груди и кашля, особенно по ночам и ранним утром. Эти эпизоды обычно связаны с распространенной, но изменяющейся по своей выраженности обструкцией дыхательных путей в легких, которая часто бывает обратима, либо спонтанно, либо под действием лечения (GINA, 2006).
В последних международных документах развивается концепция о нецелесообразности выделения степени тяжести БА для обычной клинической практики и целесообразности перехода на деление БА по уровню контроля. Классификация БА по степени тяжести рекомендуется только для научных целей. Однако, по мнению экспертов РРО, учитывая важность первоначальной оценки тяжести БА, а также социальные и экспертные особенности нашей страны, целесообразно сохранение классификации по степени тяжести БА для РФ. Тяжесть БА традиционно определялась как внутренний индивидуальный уровень активности болезни. Наиболее правильная оценка тяжести БА может быть сделана только перед началом терапии или какого- либо вмешательства (элиминационные мероприятия). Итак, по степени тяжести БА делится на интермиттирующую, легкую, среднетяжелую и тяжелую персистирующую (табл.1).
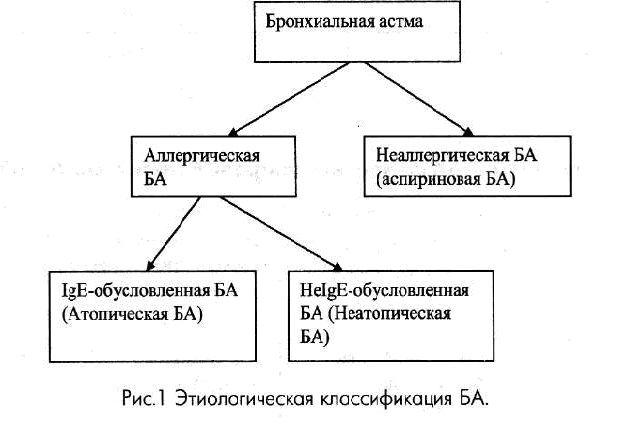
В соответствии с последней номенклатурой аллергических болезней, астму, опосредованную иммунологическими механизмами, следует называть аллергической астмой. Аллергические механизмы имеют преобладающее значение почти в 80% случаев детской астмы и более чем в 50% случаев у взрослых. Если доказано участие 1дЕ антител в формировании астмы, то следует обозначать ее IgE - опосредованной аллергической астмой. В нашей стране эту форму бронхиальной астмы принято называть атопической. Термин атопия следует использовать только после документированного подтверждения IgE сенсибилизации: выявлением специфических IgE антител в сыворотке крови или положительными результатами кожных тестов с аллергенами, то есть проведения специфического аллергологического обследования, кото¬рое выполняется только врачом аллергологом- иммунологом.
В GINA, 2006 рекомендована классификация БА по уровню контроля с выделением контролируемой, частично-контролируемой и неконтролируемой БА (табл.2). Такой подход лучше описывает состояние болезни относительно проводимых лечебных мероприятий, отражает понимание того, что тяжесть БА зависит не только от выраженности симптомов заболевания, но и от ответа на терапию и что у конкретного пациента степень тяжести может изменяться в течение нескольких месяцев или лет. Контроль БА может достаточно быстро изменяться в ответ на воздействие триггеров или проводимую терапию, и хотя он частично определяется тяжестью болезни, он также включает оценку адекватности проводимой терапии.
Примеры формулировки диагноза БА:
Бронхиальная астма, атопическая форма, легкого персистирующего течения, частично- контролируемая. Интермиттирующий аллергический ринит, ремиссия. Аллергический конъюнктивит, ремиссия. Аллергия к клещу домашней пыли, шерсти домашних животных (кошка).
Классификация БА по степени тяжести.
Таблица 1.
Характеристики Интермиттирующая БА Легкая персистирующая БА Среднетяжелая персистирующая БП Тяжелая персистирую- щая БА Дневные симптомы Реже 1 раза в неделю Чаще 1 раза в нед., но реже 1 раза в месяц Ежедневные Ежедневные Обострения Кратковременные Могут нарушать активность и сон Могут нарушать активность и сон Частые Ночные симптомы S 2 раз в месяц Чаще 2 раз в месяц >1 раза в неделю Частые Ограничение физической активности ОФВ1 или ПСВ >80% от должных значений 80% от должных значений 60-80% от должных значений 260% от должных значений Вариабельность ПСВ или ОФВ1 <20% 530% >30% >30%
Классификация БА по уровню контроля болезни (GINA, 2006)
Таблица 2.
Характеристики Контролируемая БА (все нижеперечисленное) Частично- контролируемая БА (любое проявление в течение любой недели) Неконтролируемая Б А Дневные симптомы Отсутствуют или S2 эпизодов в неделю > 2 эпизодов в неделю
Наличие трех или более признаков частично- контролируемой БА в течение любой недели
Отсутствуют Любые Наличие трех или более признаков частично- контролируемой БА в течение любой недели Ночные симптомы/ пробуждения Отсутствуют Любые Наличие трех или более признаков частично- контролируемой БА в течение любой недели Потребность в препаратах неотложной помощи Отсутствуют или S2 эпизодов в неделю > 2 эпизодов в неделю Функция легких (ПСВ или ОФВ1) Нормальная <80% от должного или наилучшего значения для данного пациента Обострения Отсутствуют 1 или более в год 1 в течение любой недели
Бронхиальная астма, атопическая форма, среднетяжелого персистирующего течения, контролируемая. Персистирующий аллергический ринит, медикаментозная ремиссия. Аллергический конъюнктивит, ремиссия. Аллергия к клещу домашней пыли, шерсти домашних животных (кошка, собака), пыльце деревьев, злаковых трав. Перекрестная пищевая аллергия к моркови, яблокам, косточковым.
Бронхиальная астма аспириновая, тяжелого персистирующего течения, неконтролиремая, обострение. Эмфизема легких. Пневмосклероз. ДНН. Полипозный риносинусит. Непереносимость АЦСК и НПВС (Аспириновая триада).
Бронхиальная астма, неатопическая форма, среднетяжелого персистирующего течения, частично-контролируемая.
БРОНХИАЛЬНАЯ ACTМА И ДРУГИЕ АТОПИЧЕСКИЕ БОЛЕЗНИ
Атопия - это генетическая предрасполо¬женность к синтезу lgE-антител в ответ на низкие дозы аллергенов, как правило, белковой природы, причем большая часть популяции не развивает IgE сенсибилизацию в ответ на воздействие этих естественных экзоаллергенов. В настоящее время известно около 20 генов, уча¬ствующих в развитии атопии. Для многих генов определена их локализация и связь с тем или иным признаком атопии. Они обнаружены на 4,5,6,7,11 и 14 хромосомах. Определенный набор генов, который передается по наследству, составляет основу развития атопии. Однако эта наследственная предрасположенность к атопии приводит к клиническим проявлениям (астме, риниту, конъюнктивиту, экземе и анафилаксии) только под воздействием соответствующих факторов внешней среды, а именно, аллергенов.
К наиболее распространенным внешним аллергенам относятся пыльца растений (деревьев, злаковых и сорных трав) и споры непатогенных плесневых грибов (Alternaria и Cladosporium). Содержание спор этих грибов в воздухе, равно как и пыльцы, носит строго сезонный характер: с ранней весны до поздней осени. Споры исчезают с первыми морозами и практически отсутствуют в воздухе в зимнее время. К аллергенам помещений, вызывающим атопические заболевания, относятся аллергены домашней пыли, аллергены животных, аллергены тараканов, а также плесневые и дрожжевые грибы (Aspergillus, Penicillium, Candida, Rizopus). Домашняя пыль могокомпонентный аллерген: она включает в себя эпидермис человека и домашних животных, споры грибов, пыльцу растений, частицы тел, личинки, экскременты домашних насекомых, неорганические компоненты. Однако основным сенсибилизирующим компонентом домашней пыли являются клещи - пироглифиды (Dermatophagoides pteronyssinus, D. farinae, D. microceras). Распространенность клещевой сенсибилизации составляет от 73 до 91%. Сенсибилизации к бытовым аллергенам является триггером у 85% больных астмой.
Для атопической БА характерна взаимосвязь с атопическим дерматитом и аллергическим риноконъюнктивитом. И хотя рост забо¬леваемости бронхиальной астмой был отмечен раньше, увеличение заболеваемости атопическим дерматитом и аллергическим ринитом имело аналогичную динамику. Распространенность атопического дерматита увеличилась в 2-3 раза за последние 30 лет и в настоящее время достигает уровня 10-20% детской популяции. Атопический дерматит предворяет развитие астмы и аллергического ринита и является отправной точкой для последующего развития респираторной аллергии. В исследовании, которое изучало взаимосвязь атопического дер¬матита, наличия сенсибилизации к аэроаллергенам и респираторных проявлений аллергии у детей, было выявлено, что 69% детей с ранним развитием атопического дерматита (в первые 3 месяца жизни) оказывались сенсибилизиро¬ванными к аэроаллергенам к 5-летнему возрасту. Приблизительно 40 % детей больных ато¬пическим дерматитом развивают в дальнейшем бронхиальную астму, а 30-40 % - аллергический ринит. Лечение и профилактика атопического дерматита должны быть направлены не только на предотвращение обострений кожного процесса, но и на то, чтобы предупредить развитие аллергического марша - типичной после¬довательности развития клинических симптомов атопической болезни, когда одни симптомы становятся менее выраженными (кожные), тогда как другие (респираторные) развиваются и начинают доминировать. Своевременная диагностика и правильное лечение атопического дерматита могут предотвратить дальнейшую гиперпродукцию lgE-антител и развитие аллергических реакций в коже, легких и носу.
Важность проблемы аллергического ринита (АР) обусловлена его высокой распространенностью, существенным влиянием на качество жизни пациентов, на профессиональную активность и способность к обучению, а также его тесной связью с БА. Более 500 млн чело¬век во всем мире страдают от АР. Взаимосвязи между верхними и нижними дыхательными путями хорошо известны и активно изучаются с 1990-х годов. Более 80% астматиков имеют ринит и от 10 до 40% больных с ринитом страдают БА. Большинство пациентов с БА отмечают сопутствующий ринит, подтверждая концепцию «одни дыхательные пути - одна болезнь». АР влияет на течение БА. Улучшение симптомов ринита сопровождается улучшением симптомов, сопутствующей бронхиальной астмы, и наоборот: ухудшение симптомов ринита ассоциировано с утяжелением и персистенцией астматических симптомов. Эта взаимосвязь происходит от единства триггерных факторов АР и БА, особенно если речь идет об атопической природе болезни. Однако недавно подобная корреляция была продемонстрирована и у неатопических пациентов. Повышенный риск развития астмы имеют пациенты с тяжелыми, персистирующими симптомами ринита и синусита. Пациенты, страдающие АР, имеют в три раза больше шанс заболеть бронхиальной астмой по сравнению со здоровыми лицами и, как правило, ринит предшествует формированию астмы (у 32-49% больных).
Таким образом, верхние и нижние дыхательные пути являются единым целым, вовлекающимся в воспалительный процесс, который может поддерживаться или усиливаться с помощью механизмов внутренних связей, существующих между верхними и нижними дыхательными путями. Именно на этой концепции основывается международный документ ВОЗ - ARIA «Аллергический ринит и его влияние на бронхиальную астму». Следовательно, когда речь идет о диагнозе аллергический ринит или бронхиальная астма, необходимо проведение обследования как верхних, так и нижних дыхательных путей.
ВОЗ ARIA рекомендует:
Больные с персистирующим аллергическим ринитом должны быть тщательно обследованы на наличие бронхиальной астмы: анамнез, физикальное обследование, исследование функции внешнего дыхания на предмет выявления обструкции бронхов и ее обратимости.
У пациентов с бронхиальной астмой необходимо проводить соответствующую диагностику аллергического ринита: анамнез, осмотр ЛОР врача и проведение передней риноскопии, проведение специфической аллергологической диагностики врачом аллергологом.
Раннее лечение аллергического ринита может помочь предотвратить развитие бронхиальной астмы и уменьшить тяжесть ее проявлений.
У больных бронхиальной астмой и аллергическим ринитом важно использовать комбинированное лечение верхних и нижних дыхательных путей.
КЛИНИЧЕСКАЯ ОЦЕНКА БРОНХИАЛЬНОЙ АСТМЫ
Типичные симптомы БА, отмечаемые боль¬шинством пациентов, включают: экспираторную одышку, свистящее дыхание, кашель и заложенность в груди. Проявления БА вариабельны по своей интенсивности, частоте развития и зависят от контакта со специфическими аллергенами и другими триггерами, противоастматической терапии, сопутствующих заболеваний. Наиболее часто симптомы БА проявляются ночью или сразу после пробуждения, а также после физической нагрузки, что зачастую приводит к ограничению физической активности пациентов. Воспаление и гиперреактивность дыхательных путей являются ключевыми патофизиологическими признаками БА. Механизмы, лежащие в основе симптомов БА, представлены в табл. 3.
Исследования ночной астмы показали, что развитие ночных просыпаний из-за симптомов БА связаны с ухудшением эозинофильного воспаления и БГР. Так как воспаление и БГР лежат в основе патогенеза БА, это послужило основанием механистического объяснения важности ночных пробуждений из-за БА. Однако, дальнейшая экспертная оценка важности различных симптомов и их комбинации для клинической оценки БА показала, что ночные просыпания из-за симптомов БА имеют более чем 90% уровень значимости. За ними следуют: ограничение физической активности, симптомы после утреннего пробуждения и свистящее дыхание. Дополнительная польза клинической оценки симптомов БА - это определение их прогностического значения в отношении обострения БА. В исследовании 400 обострений БА было изучено ложно-положительное (симптом наблюдался, но за ним не следовало развитие обострения) значение симптомов БА в отношение дальнейшего развития обострения. Этот анализ показал, что ночные просыпания из-за астмы имеют наименьшее ложно-положительное значение (<10%) и стало быть являются высокоспецифичным предвестником развития обострения БА. Дневные симптомы БА имели 30% уровень ложно-положительного значения.
Механизмы развития симптомов БА.
Таблица 3.
Симптом Механизм Кашель Раздражение ирритантных рецепторов, бронхоконстрикция Свистящее дыхание Бронхоконстрикция Заложенность в груди Сужение мелких дыхательных путей, воздушные ловушки Одышка Увеличение работы дыхания Ночные симптомы Воспаление, бронхиальная гиперреактивность
Значимость физикального осмотра определяется фазой болезни. Она ограничена в случае интермиттирующей или стабильной контролируемой БА, когда результаты осмотра пациента никакой патологии не выявляют. Удлиненный выдох и сухие свистящие хрипы - наиболее типичные находки при аускультации пациента с БА. При обострении БА физикальный осмотр - важная часть оценки тяжести обострения, которая в свою очередь является определяющим для подбора терапии. Выраженность одышки, участие вспомогательных мышц в акте дыхания, втяжение межреберных промежутков, мозаичность аускультативной картины в легких и тахикардия - каждый из этих симптомов указывает на тяжесть обструкции.
Важным этапом клинической оценки БА явля¬ется оценка внелегочных проявлений аллергии, прежде всего, аллергического ринита, конъюнктивита, атопического дерматита. Затрудненное носовое дыхание при соответствующих жалобах и анамнезе, свидетельствуют в пользу аллергического (или неаллергического) ринита. Гиперемия конъюнктив, также в сочетании с жалобами и анамнезом, скорее всего, означает аллергический конъюнктивит. Сухость кожи в сочетании с полиморфными кожными элементами (папулы, везикулы, корочки, экскориации, лихенизация) и выраженным зудом - атопический дерматит. Наличие внелегочных проявлений атопическо¬го синдрома при соответствующем астматиче¬ском анамнезе и жалобах, делает диагноз БА практически неоспоримым.
ПРИНЦИПЫ ДИАГНОСТИКИ БРОНХИАЛЬНОЙ АСТМЫ
Астма является клиническим диагнозом, который устанавливает доктор на основании жалоб и анамнестических данных пациента, кпинико-функционального обследования с оценкой обратимости бронхиальной обструкции, специфического аллергологического обследования и исключения других заболеваний. Начало заболевания БА в большинстве случаев приходится на детский и юношеский возраст. Однако дебют болезни может быть в любом возрасте и начало болезни у взрослых и даже пожилых пациентов не является редкостью. Вместе с тем, бронхообструктивный синдром, впервые развившийся в пожилом возрасте, требует проведения дифференциальной диагностики с целым рядом сходных по клиническому течению заболеваний (ХОБЛ, тромбоэмболия легочной артерии, острая левожелудочковая недостаточность, пневмоторакс, опухолевый процесс в легких и бронхах, гипервентиляционный синдром, синдром ночного апное).
Жалобы и анамнез. Приступы затрудненного дыхания по ночам, ранним утром или после физической нагрузки, сопровождающиеся экспираторной одышкой, свистящими хрипами, приступообразным кашлем сухим или с трудноотделимой мокротой. Эти симптомы могут проходить самостоятельно или после применения лекарственных бронхолитических препаратов. Важно установить связь появления симптомов БА после контакта с аллергеном, сезонную вариабельность симптомов, сочетание с проявлениями ринита, наличие в семейном анамнезе атопии или БА.
В случае отсутствия типичных жалоб, внелегочных проявлений аллергии, и нормальной аускультативной картине, но существующем подозрении БА, необходимо задать следующие вопросы пациенту:
- Бывают ли у Вас повторяющиеся эпизоды свистящих хрипов?
- Беспокоит ли Вас кашель по ночам?
- Отмечаются ли у Вас свистящие хрипы или кашель после физической нагрузки?
- Бывают ли у Вас свистящие хрипы, заложенность в груди, кашель после контакта с аэроаллергенами или поллютантами?
- Замечали ли Вы, что простуда «спускается в грудную клетку» или продолжается больше 10 дней?
- Уменьшается ли выраженность симптомов после применения противоастматических препаратов?
Иногда встречается кашлевой вариант БА, когда единственным проявлением заболевания является кашель, беспокоящий преимущественно в ночные часы. Этот вариант БА отмечается преимущественно у детей и подростков. Кашлевой вариант БА следует дифференцировать с так называемым эозинофильным бронхитом, при котором у больных отмечается кашель и эозинофилия мокроты, однако нор¬мальные показатели спирометрии и отсутствует БГР. Кроме этого, необходимо помнить о возможности кашля, вызванного приемом препаратов ингибиторов ангиотензинпревращающего фермента (АПФ), синдром постназального за-
тека, хроническим риносинуситом и дисфункцией голосовых связок.
Значение физикального обследования обсуждалось выше.
Специальные методы диагностики БА вклю¬чают исследование функции легких с оценкой обратимости бронхиальной обструкции, выявление БГР, проведение специфического аллергологического обследования.
Исследование функции легких и оценка обратимости бронхиальной обструкции. Спирометрия является методом выбора для оценки выраженности и обратимости бронхиальной обструкции в процессе диагно¬стики и дальнейшего мониторинга БА. Объем форсированного выдоха за 1-ю секунду (ОФВ]) и форсированная жизненная емкость легких (ФЖЕЛ) являются основными показателями, отражающими степень обструкции, измеряются с использованием спирометра при форсированном выдохе.
В ходе исследования ФВД, возможно выявить тип нарушения бронхиальной проходимости (обструктивный, рестриктивный, смешанный), определить его тяжесть (легкая степень: ОФВ, >70% от должного, средняя: ОФВ, =50-60% , тяжелая: ОФВ, <50% от должного). Для определения обратимости бронхиальной обструкции проводятся пробы с бронходилататорами. Общепринятым критерием диагностики БА служит прирост ОФВ1>12% (или >200мл) по сравнению с со значением до ингаляции бронхолитического препарата.
В качестве бронходилятационных агентов рекомендовано использовать: 1) (32-агонисты короткого действия (сальбутамол, фенотерол - до 800 мкг, тербуталин - до 1000 мкг) с измерением бронходилатационного ответа через 15 мин. Положительная проба говорит об обратимости имеющих место нарушений показателей бронхиальной проходимости или о наличии скрытого бронхоспазма в случае неизмененных исходных показателей.
Пиковая скорость выдоха (ПСВ) измеряется с помощью пикфлоуметра и является важным методом диагностики (при отсутствии возможности проведения спирометрии) и оценки эффективности терапии БА. Современные пик- флоуметры отличаются портативностью, сравнительно невысокой стоимостью, простотой в обращении и являются идеальным выбором для ежедневной оценки выраженности бронхиальной обструкции пациентами в домашних условиях. Следует рекомендовать пациентам измерять ПСВ утром, сразу после пробуждения и до приема препаратов; обычно при этом получают близкое к минимальному значение ПСВ. Вечернее измерение проводится перед сном, получая более высокий показатель ПСВ. Суточную вариабельность ПСВ определяют как амплитуду ПСВ (разность между максимальным и минимальным значениями в течение дня) выраженную в процентах от средней за день ПСВ [ и усредненную за 1-2 недели. Другой метод определения вариабельности ПСВ заключается в определении минимальной за 1 неделю ПСВ (утренней) в процентах от самого лучшего в этот же период показателя (Min%Max).
Мониторинг ПСВ полезен в следующих | случаях:
- Подтверждение диагноза БА (при отсутствии возможности проведения спирометрии): Е прирост ПСВ после ингаляции бронхолитика на 60 л/мин (или на 20%) по сравнению с ПСВ до ингаляции; либо изменение ПСВ в течение [ суток более чем на 20%.
- Оценка контроля БА, особенно у больных f недооценивающих симптомы астмы. График или дневник пикфлоуметрии служат дополнительным s инструментом оценки эффективности терапии.
- Выявление факторов окружающей среды (аллергены, профессиональные факторы, физическая нагрузка, другие триггеры), провоцирующих появление симптомов БА. Для этой цели рекомендуется проведение пикфлоуметрии несколько раз в день в течение периода предполагаемого воздействия факторов риска на работе или дома, а также в период их отсутствия.
Выявление бронхиальной гиперреактивности (БГР). Наличие БГР является одним из важных критериев диагноза БА. Гипервосприимчивость дыхательных путей проявляется ; чрезмерной бронхоконстрикторной реакцией [ на различные раздражители. Основным методом измерения дыхательной гипервосприимчивости является бронхоконстрикторный тест с [ метахолином, гистамином, физической нагрузкой. Оценка результатов бронхопровокационного теста проводится по динамике ОФВг Тест считается положительным при падении ОФВ, на 20% и более (от исходного значения) после ингаляции бронхоконстрикторного агента или после физической нагрузки.
Специфическое аллергологическое обследование проводится в фазу ремиссии БА врачом аллергологом-иммунологом. Оно включает в себя: проведение кожных проб с небактериальными аллергенами, провокацион¬ных тестов с аллергенами, лабораторных тестов для определения специфических lgE-антител. В настоящее время для диагностики аллергических заболеваний применяют аппликационные, скарификационные, внутрикожные тесты и тест уколом (prick-тест). Их постановка и оценка осуществляется на коже волярной поверхности предплечья или спины по общепринятым методикам. Выбор аллергенов для тестирования и вид проб определяются результатами аллергологического анамнеза и клинической картиной заболевания. За 3-7 дней до постановки аллер- гопроб отменяются антигистаминные препараты. Проведение провокационных (назального, бронхиального, орального) тестов с аллергенами осуществляется при наличии показаний.
Учитывая высокую частоту атопической БА у детей и взрослых, каждый пациент с подозрением на БА или имеющий установленный диагноз БА должен быть проконсультирован врачом аллергологом-иммунологом, который определяет необходимость и объем специфического аллергологического обследования, а в дальнейшем - специфического лечения.
СОВРЕМЕННЫЕ ПРИНЦИПЫ ТЕРАПИИ БРОНХИАЛЬНОЙ АСТМЫ У ВЗРОСЛЫХ
К сожалению, на сегодняшний день мы не можем полностью излечить больного от бронхиальной астмы, однако мы можем добиться полного контроля над болезнью у большинства пациентов. Качество жизни этих больных может быть значительно улучшено, и не отличаться от здоровых лиц в том случае, если своевременно поставлен диагноз и назначена адекватная терапия, контролирующая астму.
Контроль БА означает контроль клинических проявлений заболевания, критерии которого определены в международном документе GINA, 2006, как
- отсутствие дневных симптомов БА (или менее 2 эпизодов в неделю)
- отсутствие ночных симптомов? отсутствие ограничений повседневной активности (включая физические упражнения)
- отсутствие потребности в препаратах неотложной помощи (или она менее 2 в неделю)
- отсутствие обострений I
- нормальная ФВД
В идеале полный контроль БА должен означать отсутствие не только симптомов болезни «нормальную функцию легких, но и отсутствие признаков воспаления в нижних дыхательных путях, ибо хорошо известно, что даже при отсутствии клинических симптомов, воспаление слизистой бронхиального дерева может сохраняться и приводить к бронхиальной гиперреактивности. Воспалительные изменения и ремодулинг (фиброзирующие изменения) бронхиальной стенки наблюдаются не только у пациентов со среднетяжелой и тяжелой астмой, но и у больных с легкой формой болезни, у которых они отличаются лишь меньшей интенсивностью. У пациентов с легкой БА могут развиваться тяжелые обострения болезни. 30-40% госпитализаций по поводу обострения БА приходится на долю пациентов с легкой формой болезни. Именно для этих пациентов характерна переоценка контроля своей астмы, использование симптоматического лечения и отсутствие адекватной противовоспалительной терапии.
Основными составляющими контроля БА являются:
- Своевременная диагностика БА и сопутствующих аллергических и неаллергических заболеваний.
- Подбор и назначение адекватной терапии для достижения и длительного поддержания контроля симптомов БА.
- Элиминационные мероприятия и мероприятия по сокращению контакта с аллергенами и другими триггерами.
- Приверженность лечению и правильная техника ингаляционной терапии.
- Отказ от курения.
- Сотрудничество между пациентом и врачом.
Обучение пациента
Бронхиальная астма не однородное заболевание. Аллергические механизмы имеют преобладающее значение почти в 80% случаев детской астмы и более чем в 50% случаев астмы у взрослых. Поэтому меры по элиминации или сокращению аллергена (аллергенов) рассматриваются как первая линия терапии, и даже когда они не могут быть выполнены полностью, они существенно редуцируют необходимую фармакотерапию (Приложение).
Как показали международные клинические исследования, на сегодняшний день достижение полного или хорошего контроля БА возможно у большинства пациентов, при условии правильной оценки тяжести, существующего уровня контроля БА и назначения адекватной противоастматической длительной базисной терапии.
Фармакотерапия - неотъемлемая часть лечения любой бронхиальной астмы. Все препараты для медикаментозного лечения астмы делятся на два вида:
- препараты неотложной помощи
- препараты базисной (постоянной) терапии.
К препаратам первой группы относятся быстро действующие |3-адреномиметики (сальбутамол, фенотерол, тербуталин, формотерол), ингаляционные антихолинергические препараты (ипратропиума бромид), комбинированные препараты ингаляционных р2-адреномиметиков и ипратропиума бромида, теофиллин короткого действия.
Ко второй группе относятся препараты, обладающие противовоспалительным действием: ингаляционные и системные кортикостероиды, кромогликат и недокромил натрия, длительно действующие 2-агонисты в комбинации с ингаляционными кортикостероидами, пролонгированные теофиллины, антагонисты лейкотриеновых рецепторов и антитела к IgE.
Эквипотентные суточные дозы ИГКС у взрослых.
Препарат Низкие дозы (мкг) Средние дозы (мкг) Высокие дозы (мкг). Беклометазона дипропионат 200 - 500 >500 - 1000 >1000 - 2000 Будесонид 200 - 400 >400 - 800 >800 - 1600 Флутиказона пропионат 100 - 250 >250 - 500 >500 - 1000 Мометазона фуроат 200 - 400 >400 - 800 >800 - 1200
Среди препаратов этой группы безусловный приоритет имеют ингаляционные глюкокортикостероиды (ИГКС). Группу ИГКС, представленных на нашем рынке, составляют: беклометазона дипропионат (торговые названия: беклазон — эко, беклазон - эко легкое дыхание, бекотид, кленил), будесонид (бенакорт, пульмикорт), флутиказона пропионат (фликсотид) и мометазона фуроат. ИГКС, составляющие основу базисной противовоспалительной терапии астмы, предотвращают развитие симптомов и обострений болезни; улучшают функциональные показатели легких; уменьшают бронхиальную гиперреактивность и некоторые компоненты ремоделинга бронхиальной стенки, в частности утолщение базальной мембраны эпителия и ангиогенез слизистой бронхов. Раннее назначение ИГКС может улучшать контроль бронхиальной астмы и нормализовать функцию легких, а также предотвратить развитие необратимого поражения дыхательных путей. Они показаны для лечения персистирующей бронхиальной астмы любой степени тяжести (Рис. 3). Степень выраженности клинических проявлений астмы и степень нарушения функции легких определяют начальную дозу ИГКС. У большинства взрослых пациентов эффект достигается при применении сравнительно низких доз ИГКС, эквивалентных 400 мкг будесонида в сутки. В таблице 4 представлены эквипотентные суточные дозы ИГКС у взрослых.
Вероятность системных эффектов ИГКС определяется их активностью и биодоступностью: при применении дозированных аэрозоле* без спейсера около 80% дозы проглатываете» и поступает в желудочно-кишечный тракт. Благодаря активной биотрансформации в печени, ИГКС обладают очень низкой системной биодоступностью (беклометазона дипропионат 20%, будесонид - 11%, флутиказона пропионат - 1%), что делает риск развития системны* эффектов незначительным. Что касается местных побочных эффектов, то они одинаковы дли всей группы ИГКС и заключаются в возможности развития кандидоза полости рта и горла, дис- фонии, возникновения рефлекторного кашля* парадоксального бронхоспазма. Предупредить возникновение этих нежелательных явлений помогают следующие мероприятия: использование спейсера, полоскание рта после ингаляции ИГКС; снижение кратности приема препарата, что существенно снижает риск развития кандидоза. Парадоксальный бронхоспазм необходимо немедленно купировать ингаляционными (2-агонистами короткого действия. Иногда предварительное (непосредственно перед ингаляцией ИГКС) применение 2-агонистов оказывается эффективным способом профилактики рефлекторного кашля и бронхоспазма и может быть рекомендовано на начальном этапе лечения ИГКС, особенно при использовании высоких доз ИГКС и выраженной бронхиальной гиперреактивности. ИГКС в низких и средних дозах редко вызывают нежелательные побочные эффекты и обладают хорошим показателем "риск/польза". Для достижения контроля бронхиальной астмы необходим длительный постоянный прием ИГКС в адекватных для данного конкретного пациента дозах. После достиже* ния стабильного контроля астмы, поддерживающая доза ИГКС подбирается индивидуально. Если контроль бронхиальной астмы стабильно поддерживается на протяжении 3 месяцев и больше, возможно уменьшение дозы ИГКС но 50%. ИГКС позволяют добиться полного контроля бронхиальной астмы, однако они не излечивают астму и прекращение приема ИГКС зачастую приводит к возвращению симптомов болезни.
Эффект ИГКС имеет дозозависимый характер и контроль болезни может быть достигнут быстрее при применении более высоких доз. Однако с повышением доз ИГКС увеличивается риск развития нежелательных побочных эффектов. Поэтому при отсутствии контроля бронхиальной астмы, добавление к ИГКС препаратов другого класса следует предпочесть увеличению доз ИГКС. Наиболее эффективной и перспективной является комбинация ИГКС и длительнодействующего 2-агониста. Это направление фармакотерапии астмы активно развивается в настоящее время: создаются и регистрируются новые комбинированные препараты. На Российском фармацевтическом рынке существуют 2-а таких препарата: саль- метерол/флутиказона пропионат (серетид) и формотерол/будесонид (симбикорт), ожидается регистрация еще одного комбинированного препарата - формотерол/беклометазона дипропионат. Создание этой группы препаратов имело строгое научное обоснование. Два разных класса препаратов, соединенные водном ингаляторе, обладают комплементарным действием на патофизиологию БА (Рис 2). ИГКС подавляет хроническое воспаление и уменьшает бронхиальную гиперреактивность |БГР), тогда как длительнодействующий (32- агонист (ДД(ЗА) не только вызывает расслабление гладких мышц бронхов, но и подавляет высвобождение бронхоконстрикторных медиаторов из тучных клеток дыхательных путей, уменьшает отек слизистой бронхов и может также подавлять активацию сенсорных нервных окончаний в бронхах.
Комбинированная терапия ИГКС и длительно действующими 2-агонистами является эффективной в лечении БА, начиная с 3-й ступени (Рис.3). Однако, в последние годы активно изучается стратегия раннего назначения комбинированных препаратов при БА. В частности, в ряде исследований показано, что сальметерол/ флутиказона пропионат в качестве стартовой поддерживающей терапии обеспечивает пациентам дополнительные клинические преимущества (улучшение функции легких, контроль симптомов) по сравнению с монотерапией ИГКС при сравнимом профиле безопасности. В июле 2008 г зарегистрировано новое показание для препарата сальметерол/флутиказона пропионат в качестве стартовой поддерживающей терапии у пациентов с персистирующей бронхиальной астмой (ежедневное возникновение симптомов, ежедневное использование средств для быстрого купирования симптомов) при наличии показаний к назначёнию препаратов кортикостероидов для достижения контроля над заболеванием.
Раннее назначение комбинированной терапии ИГКС и длительнодействующими (2- агонистами имеет ряд преимуществ. Быстрое достижение эффекта увеличивает приверженность лечению со стороны пациента, профи- лактирует развитие обострений и формирование необратимых изменений бронхиальной стенки. Кроме этого, сочетание двух препаратов в одном ингаляторе удобно для пациента и является гарантией приема противовоспалительного препарата - ИГКС.
Настоящий уровень знаний и опыт международных клинических исследований не рекомендуют использование длительнодействующих 2-агонистов в качестве систематической монотерапии при бронхиальной астме, ибо такое лечение может маскировать хроническое воспаление в нижних дыхательных путях и увеличивать риск развития тяжелых обострений бронхиальной астмы.
Системные глюкокортикостероиды не рекомендуются для поддерживающей терапии БА из-за развития побочных эффектов. Эти препараты применяются для лечения тяжелых обострений БА. Терапевтический эффект системных ГКС начинает проявляться через 4-6 часов после применения и предупреждает дальнейшее прогрессирование обострения, способствуют более быстрому разрешению обструкции. Предпочтительнее использование пероральных (таблетированных) форм системных ГКС, которые также эффективны как парентеральные формы, но легче дозируются. Стандартный короткий курс лечения обострения БА: 30-50 мг преднизолона в сутки (в 1-2 приема) в течение 5-10 дней в зависимости от тяжести обострения. После купирования симптомов обострения и возвращения функциональных показателей к обычным значениям пациента возможна отмена или постепенное снижение дозы пероральных ГКС (до полной отмены) на фоне поддерживающей терапии ИГКС.
Антилейкотриеновые препараты. Ци стеиниловые лейкотриены являются одними из важных медиаторов БА, продуцирующимися преимущественно тучными клетками и эозинофилами. Они способны вызывать бронхокон- стрикцию, повышать секрецию слизи в бронхах, сосудистую проницаемость и вызывать отек. Существует два пути угнетения активности этих медиаторов: подавление синтеза и блокада их эффектов на уровне клеток. На основании первого механизма основано действие ингибитора 5- липоксигеназы (зилеутон), второго - действие антагонистов рецепторов цистеиниловых лейкотриенов: зафирлукаста (аколат), монтелукаста (сингуляр) и пранлукаста. В России зарегистрированы: зафирлукаст и монтелукаст. Антилейкотриеновые препараты обладают слабым бронхолитическим действием, уменьшают выраженность симптомов БА, улучшают функциональные показатели, интенсивность воспаления в слизистой бронхов, снижают частоту обострений БА. Как видно из рисунка 3, они могут быть альтернативой ИГКС при легкой персистирующей БА для пациентов, категорически не желающих использовать ИГКС. Однако в качестве монотерапии, они безусловно уступают ИГКС по своей противовоспалительной активности, а стало быть и клиническому эффекту. Возможно использование антилейко-- триеновых препаратов в дополнение к ИГКС,
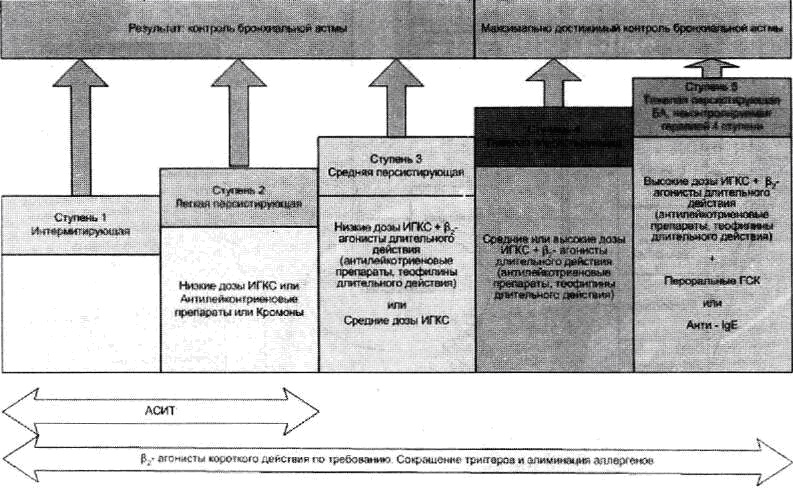
когда монотерапия ИГКС (низкими, средними или высокими дозами) недостаточна для контроля БА, хотя в ряде клинических исследований убедительно показана большая эффективность комбинации ИГКС с длительнодействующими 2-агонистами. Тем не менее, этот класс препаратов имеет свои преимущества, заключающиеся в системном противоаллергическом действии, эффективности при аспириновой БА и бронхоспазме, вызванном физической нагрузкой. Антилейкотриеновые препараты предназначены для приема внутрь, поэтому способны оказывать системные противовоспалительный, противоаллергический эффекты при сочетании БА и аллергического ринита. Они способны предотвращать развитие аспирининдуцировонного бронхоспазма у больных аспириновой БА, а также постнагрузочного бронхоспазма у больных с проявлениями бронхоспазма, вызванного физической нагрузкой. Достоинством препаратов антагонистов рецепторов цистеини- ловых лейкотриенов является их хорошая переносимость и низкая частота побочных эффектов. Взаимосвязь терапии антилейкотриеновы- ми препаратами и развитием синдрома Чердж- Стросс (системный гранулематозный васкулит), описываемая несколько лет назад ( с частотой 1 случай в год на 25000 - 150000 пролеченных пациентов ), объясняется прежде всего быстрым снижением дозы системных или ингаляционных ГКС у пациентов с тяжелой БА, что привело, по-видимому, к проявлению фонового заболевания. Однако у некоторых пациентов нельзя все же полностью исключить причинноследственной связи.
Кремоны. Кромоны - это препараты ди- натриевой соли кромоглициевой кислоты: кромогликат натрия (интал, кропоз) и недокромил натрия (тайлед). Действие этих препаратов обусловлено стабилизацией клеточной мембраны тучных клеток и торможением процесса высвобождения медиаторов аллергической реакции, развивающегося после связывания аллергена со специфическими IgEна мембране тучных клеток. До конца механизм этого действия кромонов неизвестен. Предполагают, что они блокируют кальциевые каналы мембраны тучной клетки, ингибируют фосфодиэстеразу и окислительное фосфорилирование. Кромоны подавляют активность нейтрофилов, эозинофилов, моноцитов и макрофагов, а также снижают чувствительность афферентных нервов. Эффективность кромонов при БА у взрослых незначительная, они существенно уступают ИГКС, и поэтому могут быть использованы только при легкой персистирующей БА. Причем в случае отсутствия контроля БА на фоне терапии кромонами в течение 4-х недель, необходимо назначить больному ИГКС. Достоинство этих препаратов - в их безопасности. Кромо- гликат и недокромил натрия практически полностью лишены побочных эффектов, что дает им предпочтение при лечении детей с легкой персистирующей БА.
Теофиллины длительного действия. Теофиллин является бронхолитиком и в низких дозах обладает слабым противовоспалительным действием. Теофиллины длительного действия (с замедленным высвобождением) можно принимать один или два раза в сутки внутрь. Имеющиеся на сегодняшний день данные, позволяют предположить незначительную эффективность теофиллина замедленного высвобождения в качестве первого препарата для длительного поддерживающего лечения БА. Теофиллины длительного действия могут быть использованы в комбинации с ИГКС, однако в данном случае они уступают по своей эффективности и безопасности длительнодей- ствующим р2-агонистам. Существуют следующие формы выпуска препарата теофиллина с замедленным высвобождением: теопэк (таблетки 300 мг), теотард (капсулы 200 и 350 мг), теофиллин-Н.С. (таблетки 300 мг) Средняя доза для взрослого составляет 300 мг 2 раза в сутки (из расчета 10-15 мг/кг/сут в 2 приема). К нежелательным эффектам, проявляющимся при применении высоких доз теофиллина (10 мг/кг/сут и более) относятся: тошнота, рвота, жидкий стул, нарушения ритма сердца, судороги. Побочные эффекты можно уменьшить путем тщательного подбора доз и мониторинга концентрации препарата в крови; при длительном применении побочные эффекты уменьшаются или исчезают.
Антитела к IgE.В последние годы активно изучается эффективность применения ре- комбинантных человеческих анти- 1дЕ-антител (омализумаб, ксолар) у больных аллергическими заболеваниями, в частности, средне-тяжелой и тяжелой атопической бронхиальной астмой, устойчивой к терапии ингаляционными корти- костероидами. Омализумаб (Ксолар) зарегистрирован в России. Терапевтический эффект достигается с помощью нескольких типов воздействия омализумаба. Во-первых, омализумаб связывает IgE, препятствуя его взаимодействию с FceRI(высокоаффинные 1дЕ-рецепторы на клетках воспаления). После лечения омали- зумабом уровень свободного IgEв сыворотке снижается. Кроме того, омализумаб существенно уменьшает количество рецепторов FceRIна базофилах (возможно, потому что плотность рецепторов FceRIрегулируется уровнем свободного IgEв сыворотке) и тем самым снижает чувствительность клетки к действию аллергенов. Применение анти-lgEограничивается пациентами с повышенным уровнем IgEв сыворотке. Результаты клинических испытаний показали, что при лечении омализумабом снижается интенсивность ранней и поздней фаз аллергической реакции, уменьшается количество эозинофилов в мокроте. В ходе трех больших плацебо-контролируемых исследований доказано преимущество омализумаба в качестве дополнительной терапии при лечении атопической бронхиальной астмы среднего и тяжелого течения. Наибольшая эффективность препарата проявилась при лечении больных с тяжелыми формами заболевания. Анти-lgEтерапия включена в руководство GINA2006 на 5 ступени терапии (Рис.3) в качестве дополнения к лечению ИГКС, длительнодействующими (32-агонистами и другими препаратами аллергической формы БА. Применение омализумаба ограничено из-за высокой стоимости и возможности использования только инъекционных форм, а также отсутствия результатов длительных наблюдений. Решение о проведении данного вида лечения, а также и проведение собственно анти-lgEтерапии, находится в компетенции врача специалиста (аллерголога-иммунолога или пульмонолога).
Препараты неотложной помощи
Препараты неотложной помощи показаны всем больным БА, независимо от тяжести и уровня контроля болезни, для быстрого купирования бронхоспазма и сопутствующих ему симптомов.
Ингаляционные (2-агонисты короткого действия являются препаратами выбора для купирования острого бронхоспазма, а также для профилактики бронхоспазма, вызванного физической нагрузкой. На отечественном фармацевтическом рынке эти препараты представлены сальбутамолом (асталин, венто- лин, саламал эко, саламол эко легкое дыхание, сальгим) и фенотеролом (беротек Н). Бронхорасширяющий эффект ингаляционных короткодействующих (32-агонистов наступает в течение нескольких минут. Эти препараты рекомендуется применять только по потребности, которая должна быть минимальной или отсутствовать вовсе у больных с контролируемой БА. Растущее, особенно ежедневное, применение этих препаратов указывает на потерю контроля БА и требует пересмотра терапии. Наиболее распространенными побочными эффектами короткодействующих 2-агонистов являются: тахикардия, тремор, головная боль. Эти эффекты
дозозависимые и проявляются обычно при использовании высоких доз препарата. Длительнодействующий 2-агонист формотерол, благодаря быстрому началу бронхолитического действия, также может использоваться для облегчения симптомов БА, но только у пациентов, получающих базисную противовоспалительную терапию ИГКС.
Ингаляционные антихолинергиче- ские препараты короткого действия. К этой группе препаратов относятся ипратропия бромид (атровент) и окситропия бромид. Ипратропия бромид менее эффективен в отношении купирования бронхоспазма, чем короткодействующие 2-агонисты. Бронхолитическое действие его развивается медленно и начинает проявляться с 30-40 минуты. Ипратропия бромид является альтернативой короткодействующим р2-агонистам для больных, являющихся высокочувствительными к побочным эффектам последних и развивающим тахикардию, аритмию, тремор при их применении. Другой альтернативой может быть применение комбинации антихолинергического препарата с короткодействующим 2-агонистом. Данные мета анализа продемонстрировали большую эффективность такой комбинации по сравнению с сальбутамолом при обострении БА. Наибольший эффект комбинированной терапии антихолинер- гическим препаратом и короткодействующим 2-агонистом наблюдается у больных с очень выраженной бронхиальной обструкцией (ОФВ1 <1,0 л или ПСВ <140 л/мин). Торговое название комбинированного препарата ипратропия бромида и фенотерола, зарегистрированного и давно применяемого в России, беродуал.
Теофиллин короткого действия. В России традиционно применяют теофиллин короткого действия (эуфиллин) для купирования острого приступа удушья или обострения БА. Однако многочисленными клиническими исследованиями показано бесспорное преимущество в этом отношении короткодействующих 2-агонистов. По сравнению с последними, теофиллин обладает слабым бронхорасширяющим свойством, а его терапевтическая доза почти iравна токсической. Добавление теофиллина к адекватным дозам короткодействующих 2-агонистов может не сопровождаться дополнительным бронхорасширяющим эффектом, но может стимулировать акт дыхания. Теофиллин короткого действия не рекомендуется назначать пациентам, получающим теофиллин с замедленным высвобождением, либо необходим мониторинг концентрации теофиллина в сыворотке крови. Дабы избежать передозировки и развития побочных эффектов.
Способы доставки лекарственных препаратов
Лекарственные средства для лечения БА могут назначаться различными путями (peros, парентерально, ингаляционно). Безусловным преимуществом обладает ингаляционная терапия, которая позволяет быстро достигать необходимой лечебной концентрации препарата в трахеобронхиальном дереве при незначительном системном воздействии. В настоящее время существует несколько типов ингаляционных систем доставки лекарственных препаратов: дозированные аэрозольные ингаляторы (ДАИ), дозированные порошковые ингаляторы (ДПИ) и небулайзеры.
Первый дозированный аэрозольный ингалятор - Медихалер был создан в 1956 году. В качестве пропеллента (газ толкатель) в нем был использован хлорфторуглерод (ХФУ), чаще называемый фреоном. В последующие годы ДАИ, содержащие фреон стали самыми популярными, эффективными и безопасными формами лекарственных препаратов для лечения бронхиальной астмы, несмотря на некоторые очевидные недостатки. К последним относится, прежде всего, необходимость координации медленного глубокого вдоха с нажатием на клапан ДАИ, то есть с его активацией. Несовершенство техники владения ДАИ приводит к неизбежным потерям лекарственного препарата и, соответственно, к неполноценному лечению. Между тем более 70% больных с бронхиальной астмой во всем мире используют ДАИ, считая их наиболее удобными и эффективными. Активируемые дыханием ДАИ не требуют координации вдоха с нажатием на клапан ингалятора и являются простыми и удобными в обращении. Последние годы активно разрабатываются безфрео- новые ДАИ, в которых в качестве пропеллента используется гидрофторОлканы (ГФА). Лекарственные препараты в таких ДАИ находятся в виде раствора, а не суспензии, как в фреоновых ДАИ. ГФА растворы некоторых ИГКС отличаются меньшим размером частиц, что приводит к уменьшению количества препарата, оседаемого в ротовой полости и, соответственно, к снижению побочных эффектов. ДПИ проще в использовании, чем ДАИ, однако требуют определенного усилия при вдохе, что может создавать трудности для больных с существенным нарушением функции дыхания.
Небулайзерная терапия позволяет доставлять в бронхи большие дозы препарата, обладает легкой техникой ингаляции и возможностью использования даже при тяжелом нарушении функции дыхания. Этот вид ингаляционной терапии используется при тяжелом обострении БА — астматическом статусе и не рекомендуется для постоянной поддерживающей терапии астмы.
Аллергенспецифическая иммунотерапия при бронхиальной астме
Наиболее распространенным и хорошо изученным методом АСИТ является подкожная АСИТ, когда аллергены с помощью инъекций вводятся под кожу пациента в области верхней трети, плеча. Инъекционная АСИТ доказала свою эффективность при атопической БА. Мета анализ 75 клинических исследований эффективности АСИТ при БА (общее количество пациентов 3506, с БА 3188) продемонстрировал существенную клиническую эффективность метода, проявляющуюся в сокращении симптомов астмы, потребности в бронхолитической терапии, а также значительное снижение специфической бронхиальной гиперреакивности в ответ на аллерген и снижение неспецифической бронхиальной гиперреактивности. АСИТ является единственным методом терапии, способным изменить естественное развитие болезни и это существенное преимущество АСИТ по сравнению с фармакотерапией. Своевременно проведенная АСИТ, способна предупредить трансформацию аллергического ринита в бронхиальную астму, а также переход более легких форм болезни (ринита, бронхиальной астмы) в более тяжелые. Кроме этого, эффективная АСИТ может предотвратить развитие сенсибилизации к новым аллергенам особенно у детей. Следует подчеркнуть, что чем в более раннем возрасте и при более ранних стадиях заболевания проведена АСИТ, тем выше ее лечебное действие. Клинически лечебное действие АСИТ достигается после завершения повторных 3-5 курсов лечения, но облегчение симптомов может наступить уже после первого курса.
АСИТ при бронхиальной астме показана:
- пациентам с легкой персистирующей и среднетяжелой формой болезни, при показателях ОФВ1 более 70% от должной величины после адекватной фармакотерапии
- пациентам, у которых симптомы болезни не контролируются в должной степени после элиминации аллергена и фармакотерапии
- пациентам, имеющим наряду с астматическими проявлениями, назальные симптомы
- пациентам, отказывающимся от длительного приема фармакологических препаратов
- пациентам, у которых фармакотерапия вызывает нежелательные побочные эффекты.
В ходе проведения АСИТ могут возникнуть местные и системные побочные реакции. Повышенный риск развития системный побочных реакций подкожной АСИТ имеют пациенты, страдающие БА, особенно неконтролируемой астмой. Высокая частота побочных эффектов у таких больных, по-видимому, связана с размером шокового органа (легкие) и высокой степенью бронхиальной гиперреактивности.
В настоящее время начинают широко использоваться неинъекционные методы АСИТ (назальный и сублингвальный). Неинъекционные методы АСИТ имеют ряд неоспоримых преимуществ по сравнению с подкожной АСИТ: простота и безболезненность применения, отсутствие тяжелых системных реакций, возможность самостоятельного применения аллергена в домашних условиях, экономия времени пациента, высокая приверженность лечению. При локальной АСИТ происходит максимальная стимуляция местного иммунного ответа в шоковом органе, а при всасывании аллерген оказывает воздействие на других территориях слизистой оболочки и лимфоидной ткани, опосредуя системный эффект. Мета анализ 25 двойных слепых плацебо контролируемых исследований сублингвальной АСИТ при бронхиальной астме показал эффективность метода в отношении редукции симптомов, потребности в медикаментах, улучшении респираторной функции и снижении бронхиальной гиперреактивности.
Таким образом, для каждого пациента с контролируемой атопической БА, за исключением тяжелых вариантов течения болезни, должна быть рассмотрена возможность проведения АСИТ.
МЕТОДЫ ОЦЕНКИ КОНТРОЛЯ БРОНХИАЛЬНОЙ АСТМЫ
Для БА любой степени тяжести, цель терапии достижение контроля болезни. В свою очередь, для назначения адекватной терапии необходима точная и объективная оценка уровня контроля астмы. Причем эту оценку необходимо проводить периодически и после достижения контроля болезни, для того чтобы своевременно уменьшать или увеличивать объем проводимой терапии. Исходя из определения контроля БА, представленного выше, оценка контроля должна включать следующие параметры: дневные и ночные симптомы БА, потребность в препаратах неотложной помощи, нарушение обычной ежедневной активности пациента, а также нарушение легочной функции (ПСВ, ОФВ1). В настоящее время обсуждается польза оценки, так называемых, биомаркеров - минимально инвазивных маркеров аллергического воспаления, таких как оксид азота (NO) в выдыхаемом воздухе и эозинофилы в мокроте. Однако, учитывая трудоемкость, необходимость специального оборудования и неоднозначность интерпретации результатов, эти методы требуют дальнейшего изучения для того, чтобы они могли быть рекомендованы в обычную практику. На сегодняшний день контроль БА оценивается с помощью клинико-функциональных параметров. Причем особое значение придается самостоятельной оценке контроля астмы пациентом, то есть специально разработанным вопросникам, которые полностью или частично заполняются больным. В настоящее время существуют несколько валидизированных (одобренных) инструментов для оценки уровня контроля бронхиальной астмы: Тест по контролю астмы (AsthmaControlTest, ACT), Вопросник по контролю астмы (AsthmaControlQuestionnaire, ACQ), Вопросник для оценки эффективности терапии астмы (AsthmaTherapyAssessmentQuestionnaire, ATAQ), Шкала оценки контроля астмы (AsthmaControlScoringSystem).
Инструмент для оценки контроля астмы в клин